
シャイアー・ジャパン、乾燥イオン交換樹脂処理人免疫グロブリン「ガンマガード®静注用 5g」を新発売
武田薬品工業株式会社(本社:東京都中央区、代表取締役社長 CEO:クリストフ・ウェバー)は、グループ会社のシャイアー・ジャパン株式会社(本社:東京都千代田区、代表取締役社長:グレン・スノハラ)が、「ガンマガード®静注用 5g」(一般名:乾燥イオン交換樹脂処理人免疫グロブリン、以下「ガンマガード静注用 5g」)を2019年2月4日に新発売したことをお知らせします。
ガンマガード静注用は、免疫不全症である低並びに無ガンマグロブリン血症および重症感染症の治療に用いるインタクト型静注用人免疫グロブリン製剤です。ウイルス感染に対する安全性を高めるため、Solvent/Detergent(有機溶剤/界面活性剤)処理されています。
なお、現在発売中のガンマガード静注用 2.5g製剤の供給は、2019年8月をもちまして終了致します。ガンマガード静注用 5gに切り替えることにより、利便性が向上し、患者さんの負担軽減につながります。
<ガンマガード®静注用の概要>
|
製品名 |
ガンマガード静注用 2.5g・5g |
|
一般名 |
乾燥イオン交換樹脂処理人免疫グロブリン |
|
効能・効果 |
1. 低並びに無ガンマグロブリン血症 |
|
用法・用量 |
本剤2500mg 又は5000mgをそれぞれ添付の日局 注射用水50mL又は96mLに溶解し、点滴静注又は直接静注する。直接静注する場合は、極めて緩徐に行うこと。 |
|
製品写真 |
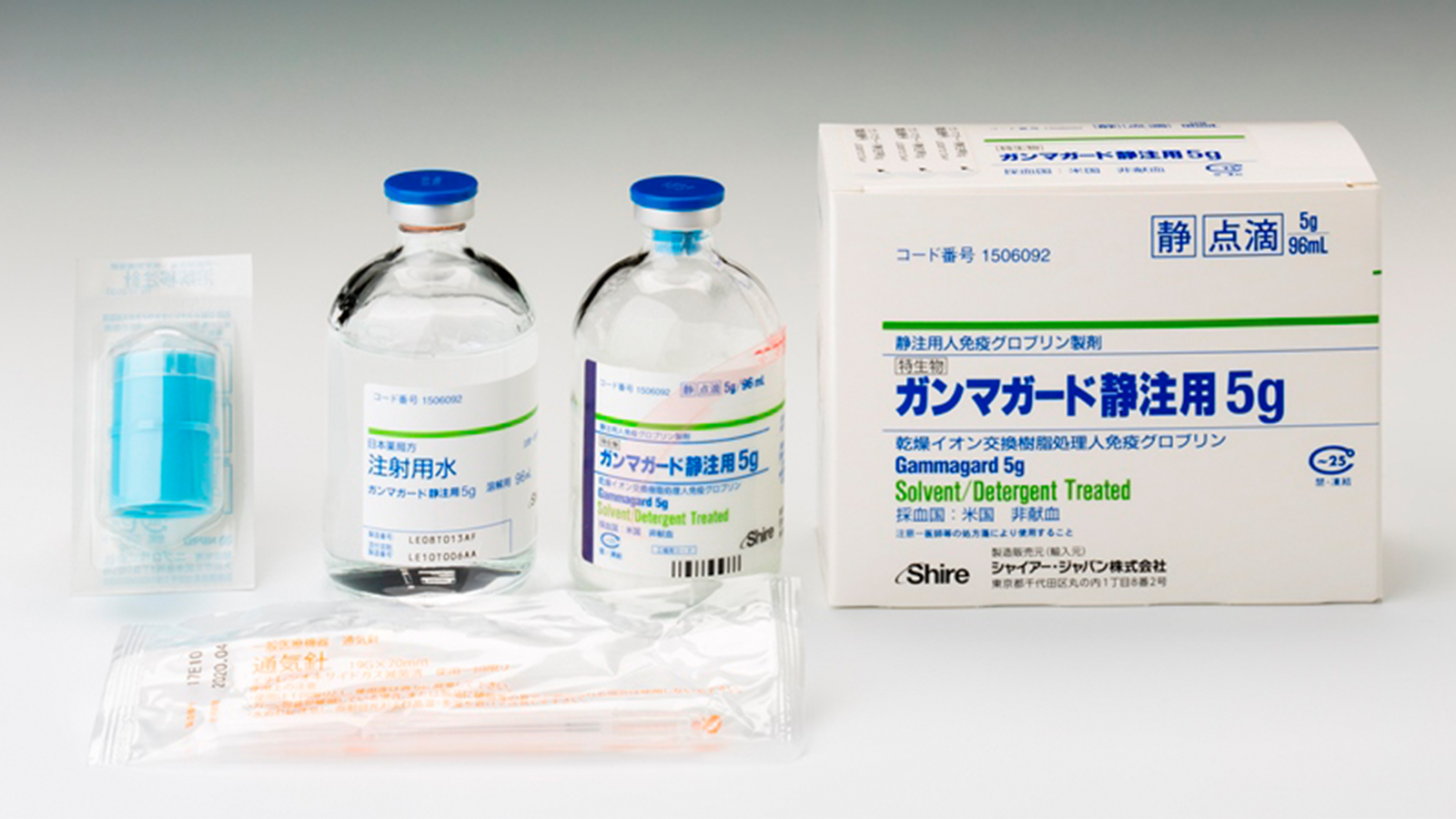 |
<無または低ガンマグロブリン血症について>
無または低ガンマグロブリン血症は、原発性と続発性(二次性)があります。原発性は、先天性のもので、続発性は、がん、ウイルス感染、放射線照射、免疫抑制剤投与などが原因で、二次的に起こります。
原発性のうち、体内で免疫グロブリンGが全く作られない場合「無ガンマグロブリン血症」と呼び、正常の約20%以下しか作られない場合を「低ガンマグロブリン血症」と呼びます。
原発性の無または低ガンマグロブリン血症の患者さんは、細菌などの感染症にかかり易くなります。このため、感染症を予防する目的で、免疫グロブリン製剤による補充療法が不可欠となります。
<注意事項>
本リリースに記載されている医薬品の情報は、当社の経営情報の開示を目的とするものであり、開発中のものを含むいかなる医薬品の宣伝、広告を目的とするものではありません。
<武田薬品について>
武田薬品工業株式会社(TSE:4502/NYSE:TAK)は、日本に本社を置き、自らの経営の基本精神に基づき患者さんを中心に考えるというバリュー(価値観)を根幹とする、グローバルな研究開発型のバイオ医薬品のリーディングカンパニーです。武田薬品のミッションは、優れた医薬品の創出を通じて人々の健康と医療の未来に貢献することです。研究開発においては、オンコロジー(がん)、消化器系疾患、ニューロサイエンス(神経精神疾患)および希少疾患の4つの疾患領域に重点的に取り組むとともに、血漿分画製剤およびワクチンにも注力しています。武田薬品は、研究開発能力の強化ならびにパートナーシップを推し進め、強固かつ多様なモダリティ(創薬手法)のパイプラインを構築することにより、革新的な医薬品を開発し、人々の人生を豊かにする新たな治療選択肢をお届けします。武田薬品は、約80の国および地域で、医療関係者の皆さんとともに、患者さんの生活の質の向上に貢献できるよう活動しています。
詳細については、https://www.takeda.com/jp/をご覧ください。
<シャイアー・ジャパンについて>
シャイアー・ジャパン株式会社は、希少疾患および特殊疾患の治療薬の開発・販売のほか、それら疾患の認知向上に力を入れています。
2019年1月8日より、シャイアーは、武田薬品のグループとなり、現在、実務的な統合を進めています。詳細については、https://www.shire.co.jp/をご覧ください。